
رغم محدودية عدد البروتينات المكتشفة مقارنةً بالعدد الهائل منها الممكن نظريًا، تمثّل هذه المجموعة المحدودة من البروتينات الأساس الوحيد الذي تستند إليه تقنيات تصميم البروتين مستقبلًا. وبالتالي، فإن دراسة مدى تمثيل هذه البروتينات للتنوّع المحتمل تُعدّ عاملًا محوريًا في توجيه استراتيجيات متعددة الاستخدامات، مثل ابتكار العلاجات، وتعزيز التحفيز الحيوي، وتصميم المواد الحيوية.
في هذا السياق، قام تعاونٌ بحثي دولي ضم معهد أوكيناوا للعلوم والتكنولوجيا (OIST)، ومعهد العلوم والتكنولوجيا النمساوي (ISTA)، وجامعة فيينا، ومركز علم الأحياء الفلكي (CAB) بدراسة الترابط بين تطوّر البروتين وفضاء التسلسلات، مع التركيز على العوامل التي تحدّ من تنوّع البروتينات.
وأظهرت نتائجهم، المنشورة في دورية الأكاديمية الوطنية للعلوم، دعمًا قويًا لنظريات إعادة تركيب الحمض النووي بوصفها قوة دافعة لتشكّل البروتينات السلفية، كما كشفت عن قيود في العديد من طرق تصميم البروتين الحديثة المعتمدة على الذكاء الاصطناعي.
ويقول البروفيسور فيودور كوندرشوف، رئيس وحدة البيولوجيا التطورية والتركيبية في المعهد: «يُنظر إلى تقنيات الذكاء الاصطناعي الحديثة بوصفها ثورة في تصميم البروتين، لا سيما بعد منح جائزة نوبل في الكيمياء لعام 2024 للفريق المطوّر AlphaFold. إلا أن معظم هذه الأساليب تُدرّب على قواعد بيانات للبروتينات المعروفة. لذلك، ما لم نفهم مدى تمثيل هذه البيانات لفضاء التسلسلات، سيبقى السؤال قائمًا إلى أي حد يمكن الوثوق بقدرة هذه النماذج على إنتاج تصميمات بروتينية متنوعة حقًا؟».
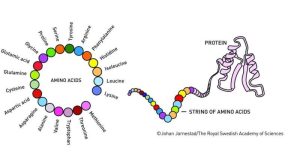
استكشاف كون البروتينات
تخيّل وجود نحو 20 نوعًا من الوحدات البنائية يمكن ترتيبها بطرق مختلفة وبأعداد متباينة ضمن سلاسل قد يبلغ طولها عشرات أو مئات أو حتى آلاف الوحدات. إن حصر جميع التركيبات الممكنة الناتجة يُشكّل ما يُعرف بفضاء التسلسل.
في حالة البروتينات، فإن الخصائص البنيوية للأحماض الأمينية تجعل جزءًا ضئيلاً جدًا من جميع التسلسلات الممكنة قادرًا على التحوّل إلى بنية ثلاثية الأبعاد صحيحة تؤدي وظيفة بيولوجية. إذ يتطلب ذلك تموضع مجموعات كيميائية محددة في المواقع الصحيحة لتكوين التفاعلات التي تحافظ على الشكل ثلاثي الأبعاد أو ترتبط بجزيئات أخرى.
ويؤدي تحديد التسلسلات التي تحقق هذه الشروط إلى تعريف فضاء وظيفي أصغر.
ومن بين هذه التسلسلات الوظيفية المحتملة، يُرجّح أن عددًا محدودًا فقط قد ظهر فعليًا عبر التاريخ التطوري. لذلك، سعى الباحثون إلى تقييم مدى تمثيل هذه المجموعة المحدودة من البروتينات للفضاء الوظيفي.
بدأ الباحثون بوصف رياضي لفضاء التسلسل الذي تشغله البروتينات المعروفة، ثم أنشؤوا نموذجًا لتطوّر البروتين لفهم العوامل البيولوجية التي تتحكم في تنوّع البنى ضمن طيف واسع من عائلات البروتين الطبيعية. ومن خلال هذه النماذج، قدّروا عدد التسلسلات الوظيفية المتوقع وجودها لوظيفة بيولوجية محددة.
وعند مقارنة تنوّع البروتينات المعروفة بهذه التنبؤات/التقديرات النظرية، تبيّن أن تأثير النقطة التي انطلقوا منها في التطوّر يفوق بكثير تأثير العمليات التطورية الأخرى.
تشير الباحثة الرئيسة لادا إيساكوفا، طالبة الدكتوراه ضمن الوحدة البحثية، إلى أن اعتبار نقطة البداية بوصفها القيد التطوّري الرئيس ليس أمرًا مفاجئًا في ذاته، إلا أن حجم تأثيرها يبدو لافتًا إلى حدٍّ كبير. وتضيف: «من منظوري كعالمة أحياء تطوّرية، فإنه لمن المثير أن يظهر الانتقاء الطبيعي والتفاعلات الجينية/الحجب الجيني (epistasis) بمساهمة ضئيلة نسبيًا في نتائجنا».
ما الذي يحدّ من تطوّر البروتينات؟
عندما تنشأ طفرات في الجينات التي تُشفِّر بروتينًا معيّنًا، فإن ذلك قد يغيّر تسلسل الأحماض الأمينية الناتج، وهو ما يقود إلى حدوث تطوّر في بنية البروتين. ويقوم الانتقاء الطبيعي بتقييد الطفرات التي تستمر عبر الزمن، وفقًا لمدى تأثيرها في تحسين وظيفة البروتين أو استقراره أو الإضرار بهما.
كما تُسهم عملية الحجب الجيني -وهي التفاعلات الجينية التي تُفضي إلى مخرجات مختلفة- في تقييد المسار التطوّري؛ إذ قد تكون بعض الطفرات ذات تأثير محدود عند حدوثها منفردة، لكنها تُحدث تأثيرات كبيرة عند اجتماعها مع طفرات أخرى محدّدة.
وعلى الرغم من أن كِلَا العاملين، الانتقاء الطبيعي والحجب الجيني، معروفان بدورهما في تشكيل تطوّر البروتينات، فإن إيساكوفا وزملاءها توصّلوا إلى أن العامل الأكثر حسمًا في تحديد تنوّع البروتينات هو أصل هذه البروتينات، حيث لوحظ وجود تباعد محدود نسبيًا عن مناطق التسلسل المرتبطة بالبروتينات السلفية.
وتسهم هذه النتائج في دعم التصوّرات العلمية المتعلقة ببدايات الحياة، لا سيما ما يتصل بآليات تكوّن البروتينات الأولى.
وتبيّن إيساكوفا أن المحاكاة تشير إلى أن نشوء البروتينات الأولى لدى السلف المشترك، لم يكن نتيجة سلسلة من الطفرات انطلاقًا من تسلسل وحيد، بل إن القيود الزمنية تجعل هذا السيناريو غير كافٍ. وبدلًا من ذلك، يُحتمل أن تكون أجزاء صغيرة من الحمض النووي قد أعيد ترتيبها ودمجها بطرق مختلفة، مما أفضى إلى تفاعلها لتكوين جزيئات جديدة من الحمض النووي قادرة على ترميز بروتينات مختلفة جذريًا.
كما يأمل الفريق البحثي أن تُحفّز هذه النتائج العلماء التجريبيين على توسيع نطاق التسلسل المعروف. وتشير إيساكوفا إلى أن الأساليب القائمة على الشبكات العصبية للتنبؤ بوظائف البروتينات تظلّ محدودة بحدود مجموعات البيانات المتاحة، ما يجعل معظم البيانات الحالية عاجزة عن التعميم خارج فضاء التسلسل المعروف حاليًا.
تختتم إيسكوفا قائلة: «هناك جزء كبير من التسلسلات لا تزال غير مكتشفة، وأن استكشافها يتطلب جهودًا وتوفير بيانات تجريبية جديدة تمكّن من التوسّع نحو هذه المناطق غير المعروفة».
ترجمة: علاء شاهين

